1.1 Le terapie con CAR-T cells: che cosa sono e come funzionano
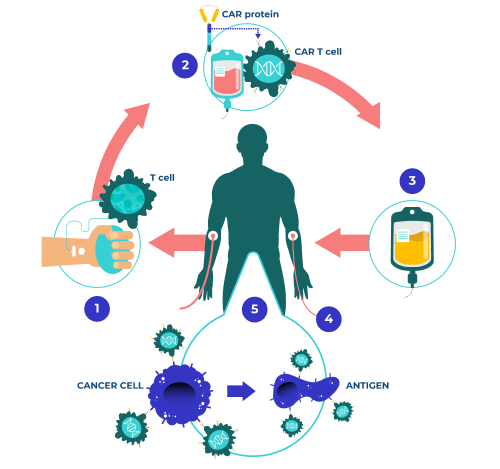
Le terapie con CAR-T (acronimo dall’inglese Chimeric Antigen Receptor T cell therapies ovvero “Terapie a base di cellule T esprimenti un Recettore Chimerico per antigene”) sono nuove terapie personalizzate contro il cancro che agiscono direttamente sul sistema immunitario del paziente per renderlo in grado di riconoscere e distruggere le cellule tumorali.
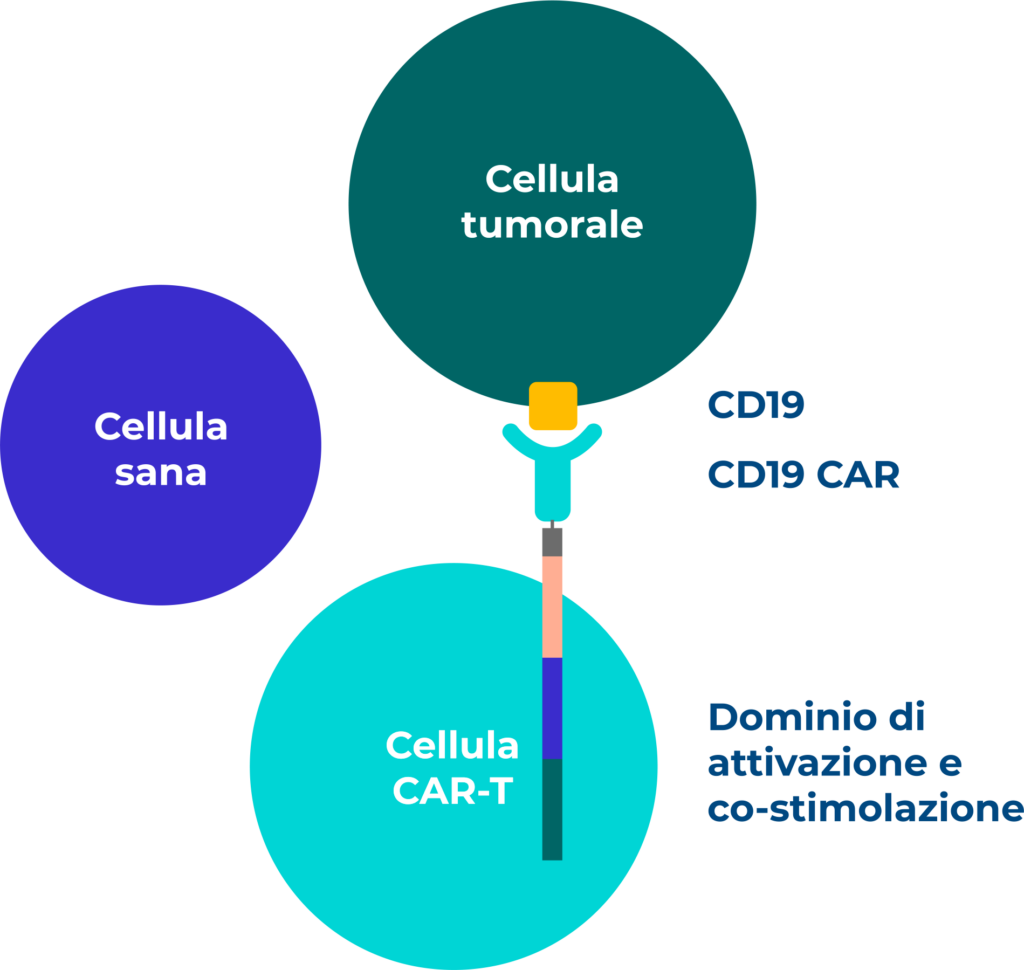
I linfociti T vengono prelevati dal paziente e modificati geneticamente in laboratorio in modo da renderli capaci di attaccare il tumore una volta re-infusi nel paziente stesso. Nella produzione in laboratorio delle cellule CAR-T, i linfociti vanno a esprimere sulla loro superficie cellulare un recettore CAR, che è chimerico in quanto costituito da 2 porzioni: una porzione extracellulare che ha il compito di riconoscere in modo selettivo un antigene delle cellule tumorali e una porzione intracellulare che, una volta che l’antigene si è legato al recettore, manda al linfocita un segnale di attivazione immediato per eliminare le cellule tumorali.
L’AZIONE DELLE CELLULE CAR-T
1.2 Chi può essere candidato a ricevere questo tipo di terapia
La terapia con CAR-T cells non è purtroppo disponibile per tutti i pazienti con malattie ematologiche. Ci sono infatti dei criteri molto accurati definiti da AIFA (Agenzia Italiana del Farmaco) che definiscono se il paziente è eleggibile per questa terapia o no.
Tali criteri tengono conto per esempio di:
- Patologia di base del paziente: al momento le CAR-T disponibili in Italia agiscono contro il CD19 e possono essere utilizzate solo in alcuni tipi di linfoma non Hodgkin e nella leucemia linfoblastica acuta B.
- Il performance status del paziente, ovvero il grado di autonomia del paziente nelle attività quotidiane.
- L’età del paziente: non è possibile a oggi eseguire queste terapia in Italia in pazienti con età superiore a 75 anni.
- La presenza di importanti alterazioni agli esami ematici
- La presenza di alcune patologie neurologiche in anamnesi
- La presenza di trombosi venosa recente
La terapia con CAR-T, come vedremo, è una terapia molto complessa e può essere eseguita solo in centri qualificati.
È quindi fondamentale che i pazienti vengano attentamente valutati da un centro qualificato, in modo che verifichi l’eleggibilità del paziente e la fattibilità di questa terapia.
1.3 Quali sono i prodotti CAR-T attualmente disponibili in Italia e con quali indicazioni
Finora l’AIFA ha autorizzato in Italia tre terapie con le cellule CAR-T che riconoscono l’antigene CD19, presente in diversi tumori del sangue.
Sono in corso di approvazione altre terapie con CAR-T sia contro il CD19 che contro altri antigeni (p. e. anti BCMA per i pazienti con mieloma multiplo).
LE TERAPIE A OGGI DISPONIBILI IN ITALIA
Seleziona l’argomento che ti interessa per avere ulteriori informazioni
Axicabtagene ciloleucel (Axi-cel)
Axicabtagene ciloleucel (Axi-cel)
è autorizzato come trattamento di persone adulte con linfoma non-Hodgkin diffuso a grandi cellule B o linfoma primitivo del mediastino a grandi cellule B. Per entrambi questi tipi di tumore, la terapia con le cellule CAR-T può essere intrapresa solo dopo che il paziente sia stato già sottoposto ad almeno due terapie senza successo.
Tisagenlecleucel (Tisa-cel)
Tisagenlecleucel (Tisa-cel)
è approvato per bambini e giovani adulti fino ai 25 anni con leucemia linfoblastica acuta a cellule B refrattaria o recidivata. Inoltre, il farmaco è stato approvato per le persone adulte con linfoma diffuso a grandi cellule B dopo che 2 linee di terapia non si siano dimostrate più efficaci.
Brexucabtagene Autoleucel (Brexi-cel)
Brexucabtagene Autoleucel (Brexi-cel)
è stato autorizzato per i pazienti adulti con Linfoma Mantellare recidivato o refrattario dopo 2 o più linee di terapia, che abbiano incluso anche terapia con Ibrutinib.
1.4 Come vengono prodotte le cellule CAR-T
Diversamente dai farmaci tradizionali, le cellule CAR-T sono dei cosiddetti “farmaci vivi” e vengono generate in maniera personalizzata ovvero utilizzando il sangue del paziente.
La produzione e la somministrazione di una terapia CAR-T richiedono una procedura complessa, che coinvolge specifiche figure professionali ed è articolata in più fasi.
Vista la complessità della procedura, queste terapie vengono infuse solo in centri che abbiano superato rigidi controlli di qualità. Per questo motivo è fondamentale uno stretto rapporto fra il centro di appartenenza (centro referral) e il centro CAR-T, al fine di ottimizzare i tempi e permettere la miglior gestione del paziente e della terapia.
LE FASI DELLA PRODUZIONE E DELLA SOMMINISTRAZIONE DI UNA TERAPIA CON CAR-T
Seleziona l’immagine per ulteriori informazioni

Prelievo
1. PRELIEVO
I linfociti T vengono prelevati dal sangue del paziente in un centro trasfusionale autorizzato, mediante un processo che consente di isolarli dal sangue periferico (leucaferesi), rimettendo in circolo i restanti elementi ematici. I linfociti T vengono successivamente inviati alla struttura che si occuperà dell’ingegnerizzazione genetica.

Ingegnerizzazione genetica
2. Ingegnerizzazione genetica
I linfociti T del paziente vengono geneticamente modificati, in strutture altamente qualificate per la produzione di terapie avanzate. Utilizzando un virus inattivato (vettore virale), viene aggiunto al DNA dei linfociti un gene ricombinante che permette di esprimere sulla superficie dei linfociti T una proteina, nota come Recettore dell’Antigene Chimerico (CAR). Grazie a questo recettore, i linfociti T modificati (CAR-T cells) sono in grado di riconoscere un antigene specifico presente sulla superficie delle cellule tumorali e legarsi a esse. Le cellule CAR-T vengono moltiplicate in laboratorio, congelate e successivamente inviate al centro che dovrà somministrare il trattamento.

Chemioterapia pretrattamento (linfodepletiva)
3. Chemioterapia pretrattamento (linfodepletiva)
Prima dell’infusione, il paziente è sottoposto a una chemioterapia di preparazione per permettere ai linfociti T modificati di espandersi e attivarsi nell’organismo.

Infusione
4. INFUSIONE
Dopo la chemioterapia, le cellule CAR-T vengono infuse nel paziente, con un procedimento simile a una trasfusione di sangue.

MONITORAGGIO
5. MONITORAGGIO
Dopo l’infusione, il paziente resta in ricovero per alcuni giorni e viene costantemente monitorato per reazioni avverse al trattamento. Nelle quattro settimane successive alla dimissione, il paziente deve comunque rimanere nei pressi di una struttura clinica qualificata per essere sottoposto a regolari controlli.
1.5 Che cos’è la linfocitoaferesi
La raccolta avviene attraverso una macchina chiamata separatore cellulare. Questa apparecchiatura utilizza la forza centrifuga per separare i linfociti da tutte le altre cellule del sangue e del plasma. Le cellule vengono raccolte in una sacca. La durata della procedura varia da paziente a paziente, solitamente ha una durata da tre a quattro ore.
Gli effetti collaterali della procedura potrebbero includere stanchezza, sensazione di pesantezza nella testa, nausea e sensazione di freddo. Alcuni pazienti potrebbero avvertire la sensazione di formicolio sulle labbra e alle estremità delle dita. È molto importante che questi segnali vengano comunicati immediatamente al personale medico.
COSA VIENE CONTROLLATO PRIMA DELL’AFERESI?
Vengono verificati gli accessi venosi e, se non adeguati, potrebbe essere necessario posizionare in catetere venoso centrale (CVC), che dovrà essere tenuto solo per la durata della procedura.
Per garantire la qualità dei linfociti raccolti, è indispensabile che il personale medico analizzi in modo dettagliato tutte le terapie che il paziente sta assumendo. È infatti indispensabile sospendere certi farmaci (per esempio il cortisone) prima di procedere alla raccolta.
1.6 Riepilogo
- Le cellule CAR-T sono dei cosiddetti “farmaci vivi” e vengono generate in maniera personalizzata ovvero utilizzando il sangue del paziente.
- Le cellule CAR-T sono i linfociti T del paziente modificati geneticamente in modo da esprimere sulla superficie una proteina, nota come Recettore dell’Antigene Chimerico (CAR) in grado di riconoscere un antigene specifico presente sulla superficie delle cellule tumorali, legarsi a esse ed eliminarle.
- Non tutti i pazienti sono eleggibili a questo tipo di terapia, è dunque fondamentale un’attenta valutazione del paziente da parte di un centro qualificato per la terapia con CAR-T.
- La produzione e la somministrazione di una terapia CAR-T richiedono una procedura complessa, che coinvolge specifiche figure professionali ed è articolata in più fasi.
- Per la produzione delle cellule CAR-T è indispensabile la raccolta dei linfociti T del paziente, che avviene tramite una procedura che si chiama linfocitaferesi.